Timeline
2019
2020
- Langen Junior Science Award
- WHO Declares Pandemic
- Paul Ehrlich and Ludwig Darmstaedter Prize
- Supply Bottleneck for Pneumococcal Vaccines
- Blood Donation Remains Possible
- Convalescent Plasma: First Clinical Trial
- COVID-19 Vaccines: First Clinical Trial
- Marketing Authorisation of Gene Therapy
- COVID-19 Vaccines: Second Clinical Trial Approved
- German Presidency of the EU Council
- COVID-19 Vaccines: Two Clinical Trials Approved
- Another Clinical Trial Approved
- Start of Two Rolling Review Procedures
- Allergen Products: European Standards
- Allergen Product: First European Marketing Authorisation
- COVID-19 Peptide Vaccine: First Clinical Trial
- COVID-19 Vaccine: Third Rolling Review Procedure
- Validation of COVID-19 Rapid Tests
- First Marketing Authorisation of a COVID-19 Vaccine
- SafeVac App Available
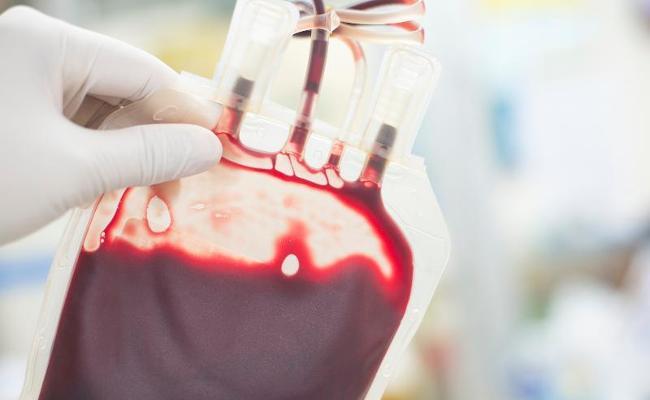
Blut und Blutprodukte sind in Deutschland sichere Arzneimittel. Expertinnen und Experten des Paul-Ehrlich-Instituts sorgen dafür, dass dies trotz bekannter und neu auftretender Erreger auch so bleibt. Seit Januar 2020 ist deshalb die Testung von Blutkomponenten zur Transfusion sowie Stammzellpräparaten auf Hepatitis E verbindlich vorgeschrieben, seit 2021 auch für gefrorene Frischplasmen.